Definisi unsur – Unsur kimia, blok bangunan dasar alam semesta, memegang peran penting dalam membentuk dunia di sekitar kita. Dari logam yang kokoh hingga gas yang tak terlihat, unsur-unsur ini adalah pemain kunci dalam membentuk materi dan menggerakkan kehidupan.
Definisi unsur kimia adalah zat murni yang tidak dapat diuraikan lebih lanjut menjadi zat yang lebih sederhana melalui reaksi kimia biasa.
Definisi Unsur Kimia

Dalam dunia kimia, unsur merupakan bagian fundamental penyusun materi. Unsur-unsur ini merupakan bahan dasar yang tidak dapat dipecah menjadi zat yang lebih sederhana melalui reaksi kimia biasa.
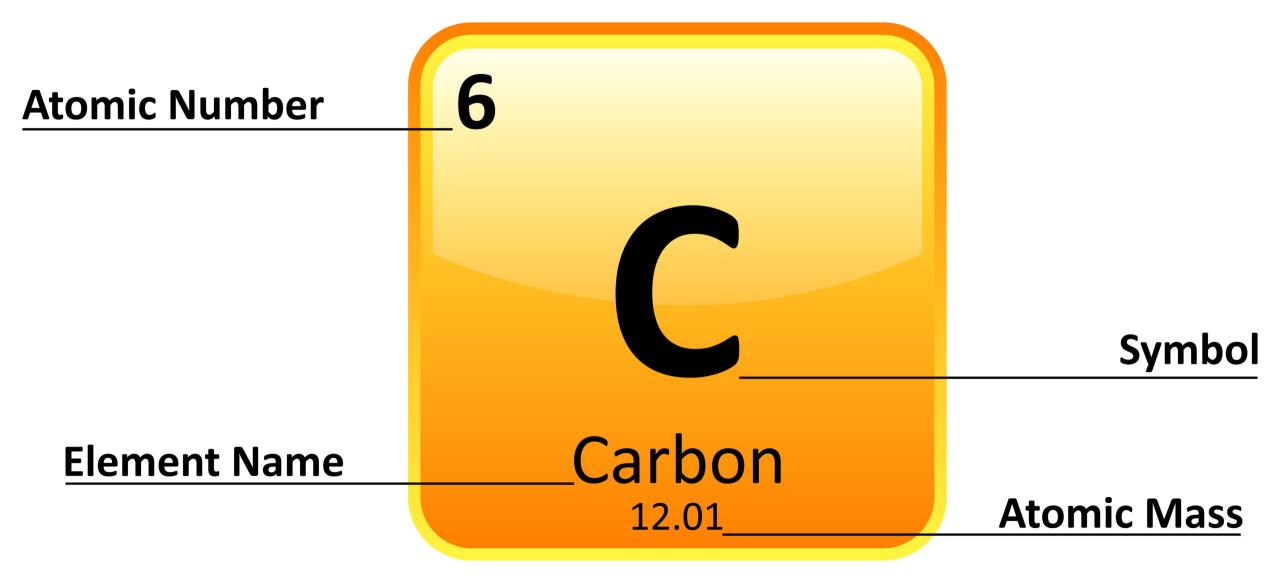
Setiap unsur memiliki karakteristik unik yang membedakannya dari unsur lainnya. Ciri-ciri khas ini meliputi nomor atom, massa atom, dan elektron valensi.
Sifat-Sifat Umum Unsur
- Nomor Atom:Menunjukkan jumlah proton dalam inti atom suatu unsur.
- Massa Atom:Rata-rata massa atom dari semua isotop suatu unsur.
- Elektron Valensi:Elektron pada kulit terluar atom yang terlibat dalam reaksi kimia.
Klasifikasi Unsur
Unsur-unsur dikelompokkan dalam tabel periodik berdasarkan sifat kimianya. Tabel periodik terdiri dari 18 kolom vertikal (golongan) dan 7 baris horizontal (periode).
Golongan menunjukkan jumlah elektron valensi, sedangkan periode menunjukkan tingkat energi elektron.
Kegunaan Unsur
Unsur-unsur memiliki beragam kegunaan dalam kehidupan sehari-hari, seperti:
- Sebagai bahan konstruksi (besi, aluminium)
- Sebagai bahan bakar (hidrogen, uranium)
- Dalam obat-obatan (yodium, natrium)
- Dalam industri makanan (oksigen, nitrogen)
Tabel Periodik Unsur

Tabel periodik unsur merupakan sebuah susunan unsur-unsur kimia dalam format tabel, yang disusun berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia yang berulang. Tabel ini merupakan alat yang sangat penting bagi para ilmuwan untuk memahami dan memprediksi sifat-sifat unsur.
Susunan Tabel Periodik
Tabel periodik disusun dalam 18 kolom vertikal, yang disebut golongan, dan 7 baris horizontal, yang disebut periode. Golongan dinomori dari 1 hingga 18 dari kiri ke kanan, sedangkan periode dinomori dari 1 hingga 7 dari atas ke bawah.
Unsur-unsur dalam tabel periodik dikelompokkan berdasarkan sifat kimianya yang serupa. Misalnya, unsur-unsur dalam golongan 1 (logam alkali) sangat reaktif dan mudah membentuk ion positif, sedangkan unsur-unsur dalam golongan 18 (gas mulia) sangat stabil dan tidak reaktif.
Tren Periodik
Tabel periodik menunjukkan tren periodik dalam sifat-sifat unsur. Misalnya, jari-jari atom (ukuran atom) umumnya meningkat dari kanan ke kiri dalam suatu periode dan menurun dari atas ke bawah dalam suatu golongan.
Elektronegativitas (kemampuan suatu atom untuk menarik elektron) umumnya meningkat dari kiri ke kanan dalam suatu periode dan menurun dari atas ke bawah dalam suatu golongan.
Keadaan oksidasi (jumlah elektron yang dapat diterima atau diberikan oleh suatu atom) umumnya meningkat dari kiri ke kanan dalam suatu periode dan menurun dari atas ke bawah dalam suatu golongan.
Penggunaan Tabel Periodik
Tabel periodik memiliki banyak kegunaan, di antaranya:
- Mengorganisir dan mengklasifikasikan unsur-unsur berdasarkan sifat kimianya.
- Memprediksi sifat-sifat suatu unsur berdasarkan posisinya dalam tabel periodik.
- Membuat perkiraan tentang reaktivitas dan perilaku kimia suatu unsur.
- Mengembangkan model dan teori tentang struktur atom dan ikatan kimia.
Klasifikasi Unsur: Definisi Unsur
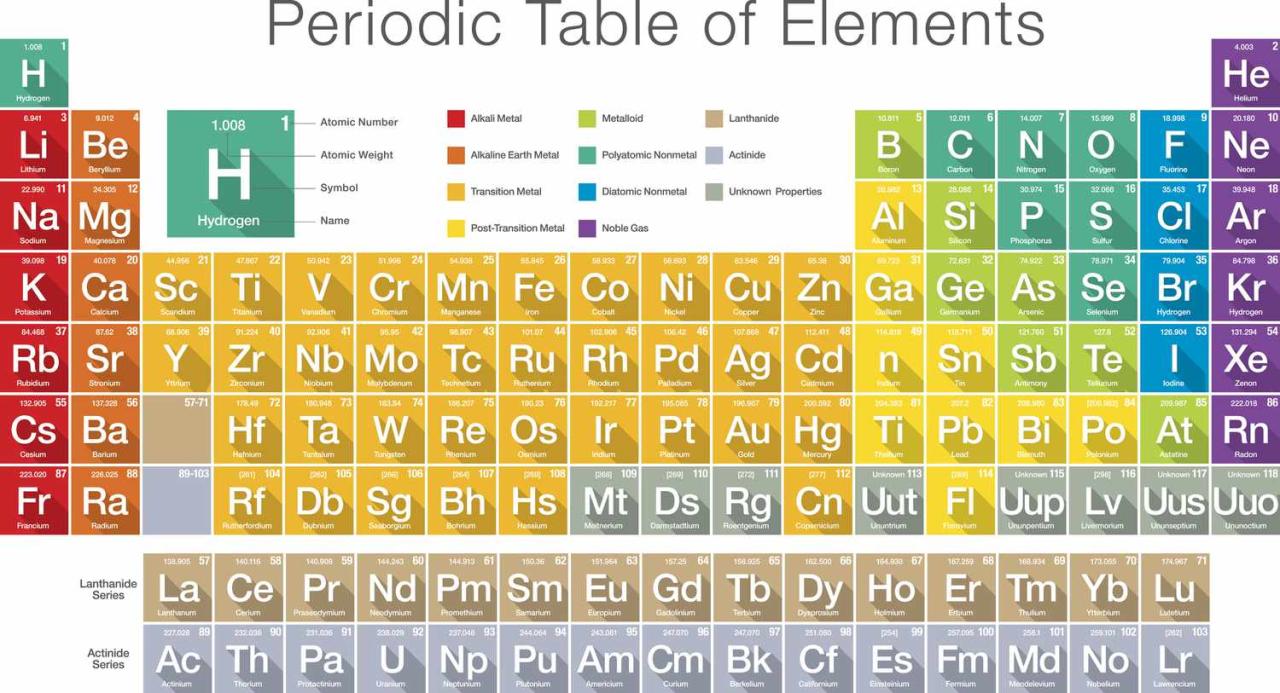
Unsur-unsur kimia yang ada di alam memiliki sifat dan karakteristik yang berbeda-beda. Untuk memudahkan pemahaman dan pengelompokan, unsur-unsur tersebut diklasifikasikan ke dalam tiga kategori utama berdasarkan sifat fisik dan kimianya: logam, non-logam, dan metaloid.
Logam, Definisi unsur
Logam merupakan unsur yang umumnya memiliki sifat mengkilap, dapat menghantarkan listrik dan panas dengan baik, serta mudah ditempa dan dibentuk. Logam juga cenderung padat pada suhu kamar, kecuali merkuri yang berwujud cair. Beberapa contoh logam yang umum ditemukan antara lain besi, tembaga, aluminium, dan emas.
Non-Logam
Non-logam adalah unsur yang memiliki sifat kebalikan dari logam. Non-logam umumnya tidak mengkilap, merupakan isolator listrik dan panas yang buruk, serta cenderung rapuh dan tidak dapat ditempa. Beberapa contoh non-logam yang umum ditemukan antara lain oksigen, hidrogen, nitrogen, dan karbon.
Metaloid
Metaloid memiliki sifat yang berada di antara logam dan non-logam. Metaloid dapat menghantarkan listrik dan panas, namun tidak sebaik logam. Metaloid juga dapat membentuk ikatan dengan logam dan non-logam. Beberapa contoh metaloid yang umum ditemukan antara lain silikon, germanium, dan arsenik.
Sifat dan Reaktivitas Unsur
Unsur-unsur dalam tabel periodik menunjukkan sifat dan reaktivitas kimia yang unik. Sifat-sifat ini sangat bergantung pada struktur elektroniknya, yang menentukan valensi, bilangan oksidasi, dan kemampuan pembentukan ikatan.
Valensi dan Bilangan Oksidasi
Valensi adalah jumlah elektron yang terlibat dalam pembentukan ikatan, sedangkan bilangan oksidasi adalah muatan hipotetis suatu atom dalam suatu senyawa. Valensi dan bilangan oksidasi penting dalam menentukan sifat ikatan dan reaktivitas unsur.
Pembentukan Ikatan
Unsur dapat membentuk ikatan kimia melalui berbagai mekanisme, seperti ikatan ionik, kovalen, dan logam. Ikatan ionik terjadi antara logam dan non-logam, membentuk senyawa ionik. Ikatan kovalen terjadi ketika atom berbagi pasangan elektron, membentuk molekul. Ikatan logam terjadi antara atom logam, membentuk struktur logam yang stabil.
Reaktivitas Unsur
Reaktivitas unsur dipengaruhi oleh beberapa faktor, termasuk energi ionisasi, afinitas elektron, dan ukuran atom. Energi ionisasi adalah energi yang dibutuhkan untuk melepaskan elektron dari suatu atom. Afinitas elektron adalah energi yang dilepaskan ketika suatu atom menerima elektron. Ukuran atom menentukan jarak antar elektron dan inti, yang mempengaruhi reaktivitas.
Reaktivitas unsur meningkat dari kiri ke kanan pada suatu periode dan dari bawah ke atas pada suatu golongan. Logam alkali dan halogen sangat reaktif, sedangkan gas mulia relatif inert.
Aplikasi Unsur dalam Kehidupan Sehari-hari
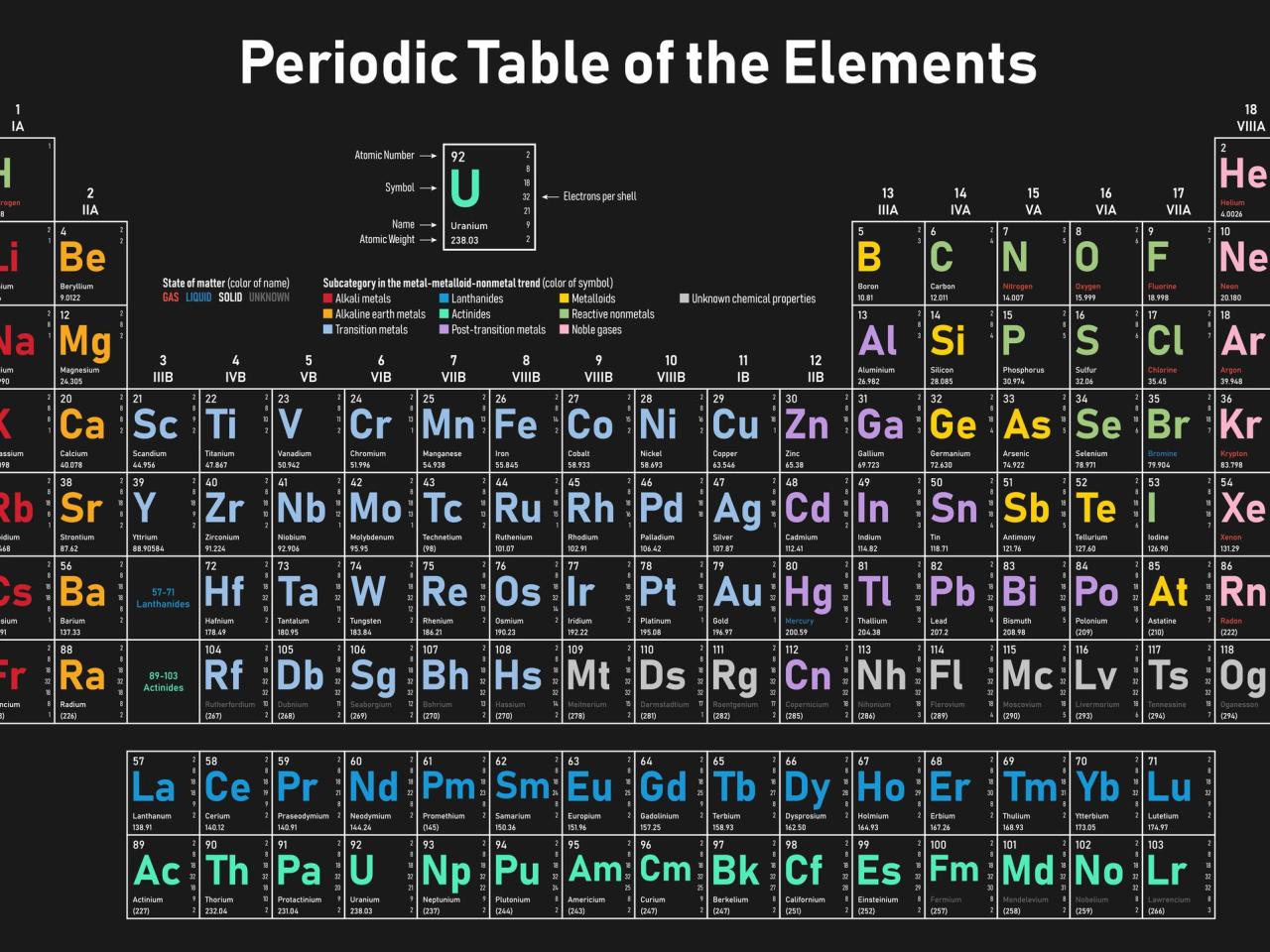
Unsur-unsur kimia memiliki peran penting dalam berbagai aspek kehidupan kita. Dari membangun rumah hingga mengobati penyakit, unsur-unsur ini membentuk dasar bagi banyak teknologi dan industri modern.
Bahan Bangunan
- Besi: Digunakan dalam konstruksi baja, peralatan, dan kendaraan.
- Aluminium: Digunakan dalam bingkai jendela, panel dinding, dan pesawat terbang.
- Tembaga: Digunakan dalam pipa ledeng, kabel listrik, dan atap.
- Kalsium: Digunakan dalam semen dan beton.
Obat-obatan
- Natrium: Penting untuk mengatur keseimbangan cairan dalam tubuh.
- Kalium: Berperan dalam fungsi saraf dan otot.
- Kalsium: Penting untuk kesehatan tulang dan gigi.
- Yodium: Mencegah gangguan tiroid.
Elektronik
- Silikon: Digunakan dalam chip komputer dan panel surya.
- Tembaga: Digunakan dalam kabel dan sirkuit listrik.
- Aluminium: Digunakan dalam kapasitor dan pendingin.
- Emas: Digunakan dalam konektor dan sakelar.
Energi
- Uranium: Digunakan dalam pembangkit listrik tenaga nuklir.
- Litium: Digunakan dalam baterai kendaraan listrik.
- Hidrogen: Digunakan sebagai bahan bakar alternatif.
- Karbon: Digunakan dalam bahan bakar fosil dan energi terbarukan.
Kesimpulan Akhir
Memahami definisi unsur tidak hanya memperluas pengetahuan kita tentang alam tetapi juga memberdayakan kita untuk memanfaatkan kekuatannya untuk kemajuan manusia. Dari teknologi inovatif hingga obat-obatan yang menyelamatkan jiwa, unsur-unsur terus membentuk dan meningkatkan kehidupan kita.
